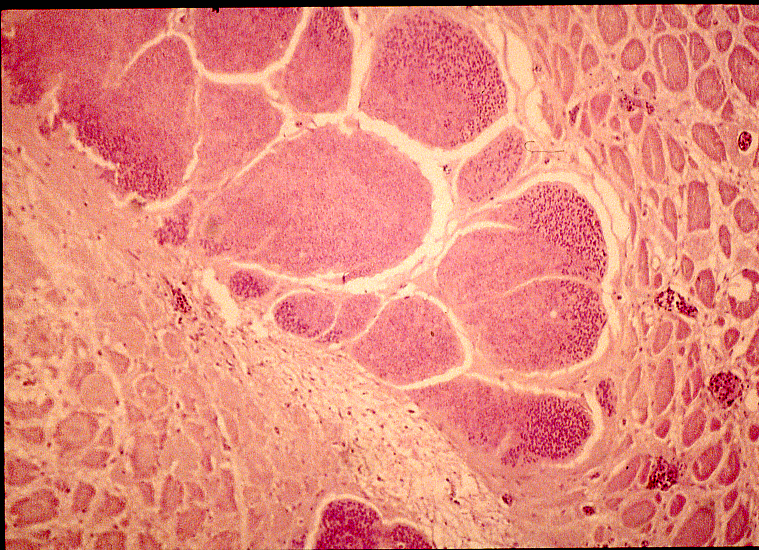

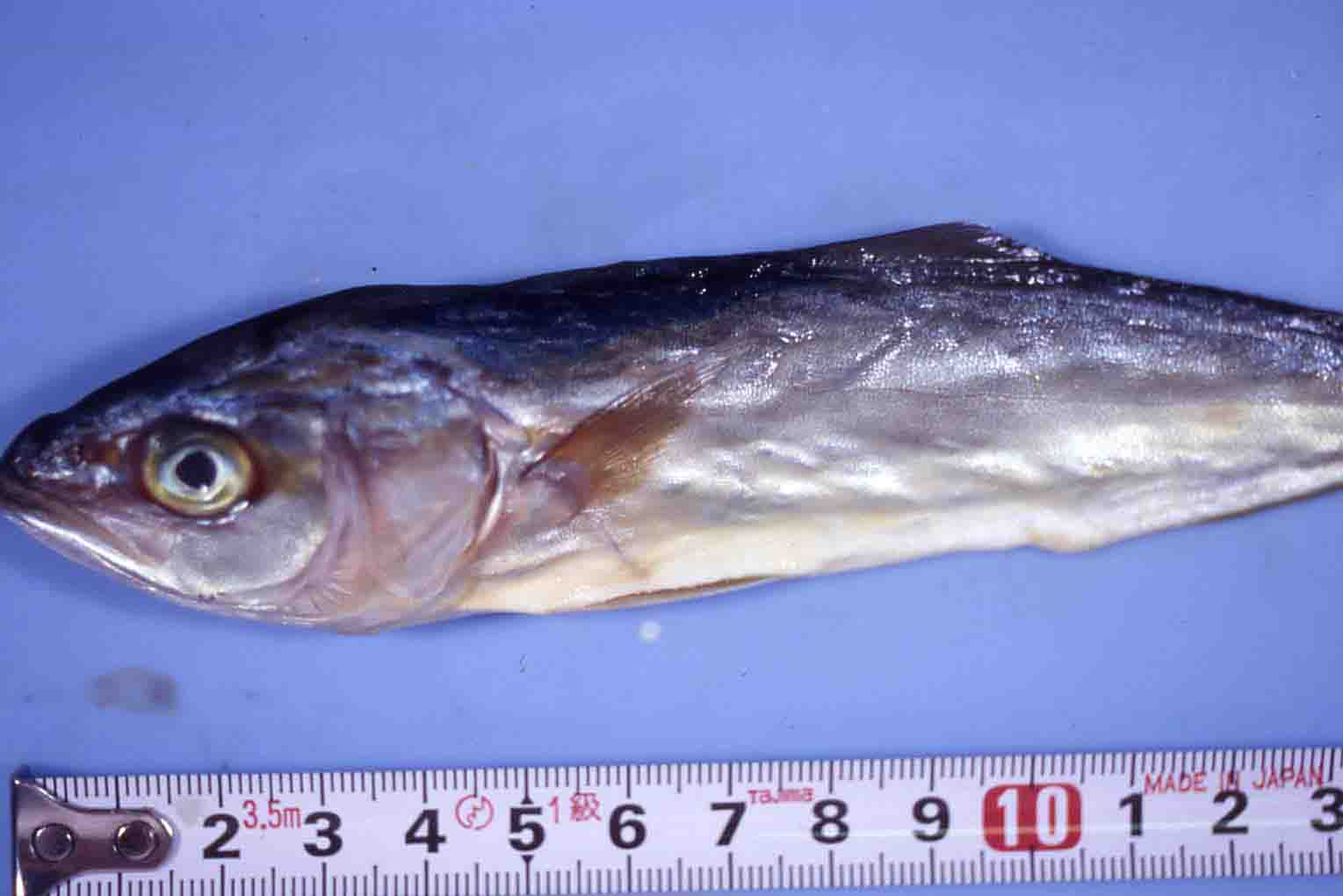
写真1.べこ病を呈したブリ稚魚の外観
写真5.胞子スタンプ標本のUvitex 2B染色像
写真4.筋肉に形成されたシストの組織
写真2.重篤寄生魚の剖検
| 寄生虫名 | Microsporidium seriolae(ブリ筋肉微胞子虫) |
|---|---|
| 分類学 | 微胞子虫門、微胞子虫綱、微胞子虫目 |
| 宿主名 | ブリ(Seriola quinqueradiata)、カンパチ(Seriola dumerili)、ヒラマサ(Seriola lalandi) |
| 病名 | べこ病 |
| 寄生部位 | 体側筋肉 |
| 肉眼所見 | 筋肉内に小シスト集塊(数mm-1 cm)が形成され、外観的に凹凸を呈する(写真1)。シストは不定形で、白色である(写真2)。 |
| 寄生虫学 | シスト内部に多数の胞子が形成される(写真3)。胞子は長さ2.9-3.7 μm、幅1.9-2.4 μm。 |
| 病理学 | 筋肉組織内のシストは宿主由来の薄い結合組織に被包されており、内部では寄生体の増殖と胞子形成が行われる(写真4)。シストの発育中には宿主反応はほとんど見られないが、胞子形成が終了するとシストは崩壊し、周囲の筋組織が広範に融解壊死する。その結果、本症の病名の由来となった体表の凹凸が生じる。重度の寄生を受けた魚は死亡することもある(小川, 2004)。一方で、シストの崩壊によって周囲の筋肉組織に放出された胞子は貪食細胞によって活発に貪食され、患部は次第に萎縮して回復する(Sano et al., 1998) |
| 人体に対する影響 | 人間には寄生しないので、食品衛生上の問題はない。 |
| 診断法 | シストをつぶしてウェットマウントで胞子を確認する。標本はスメアにしてUvitex 2B染色し、蛍光顕微鏡で観察する(Yokoyama et al., 1996)。染色された胞子は、紫外光で青い蛍光を発する(写真5)。PCRによる検出法も開発されている(Bell et al., 1999)。高感度であり感染初期の検出には適しているが、特異性に問題を残しているためPCRのみでの診断は出来ない。 |
| その他の情報 | 本病は稚魚期の病気であり、採捕直後のモジャコに見られることもあるが、一般的には生け簀内に収容してしばらく飼育してから病徴が発現する。砂濾過海水を用いた沖出し前の陸上飼育の間はほとんど感染しないことから、砂濾過には予防効果があると考えられる(Sano et al., 1998)。生活環は不明であり、魚から魚への伝播は起こらない。 |
| 参考文献 | Bell.
A. S., H. Yokoyama, T. Aoki, M. Takahashi and K. Maruyama (1999): Single and
nested polymerase chain reaction assays for the detection of Microsporidium seriolae (Microspora),
the causative agent of ‘Beko’ disease in yellowtail Seriola quinqueradiata. Dis.
Aquat. Org., 37, 127-134. 小川和夫 (2004): 原虫病. 魚介類の感染症・寄生虫病(若林久嗣・室賀清邦編), 恒星社厚生閣, pp.285-338. Sano, M., J. Sato and H. Yokoyama (1998): Occurrence of beko disease caused by Microsporidium seriolae (Microspora) in hatchery-reared juvenile yellowtail. Fish Pathol., 33, 11-16. Yokoyama, H., J.-H. Kim, J. Sato, M. Sano and K. Hirano (1996): Fluorochrome Uvitex 2B stain for detection of the microsporidian causing beko disease of yellowtail and goldstriped amberjack juveniles. Fish Pathol., 31, 99-104. |


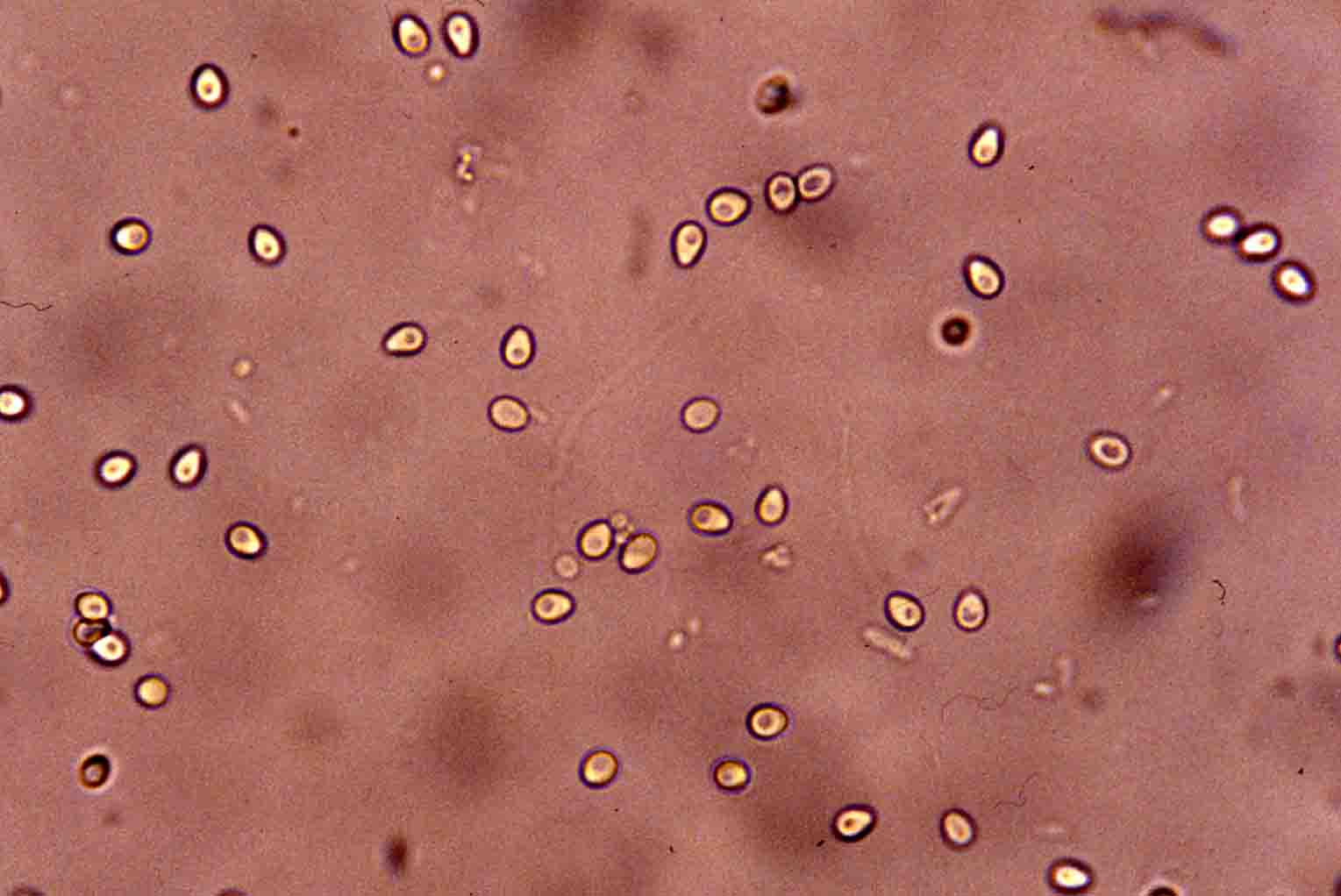
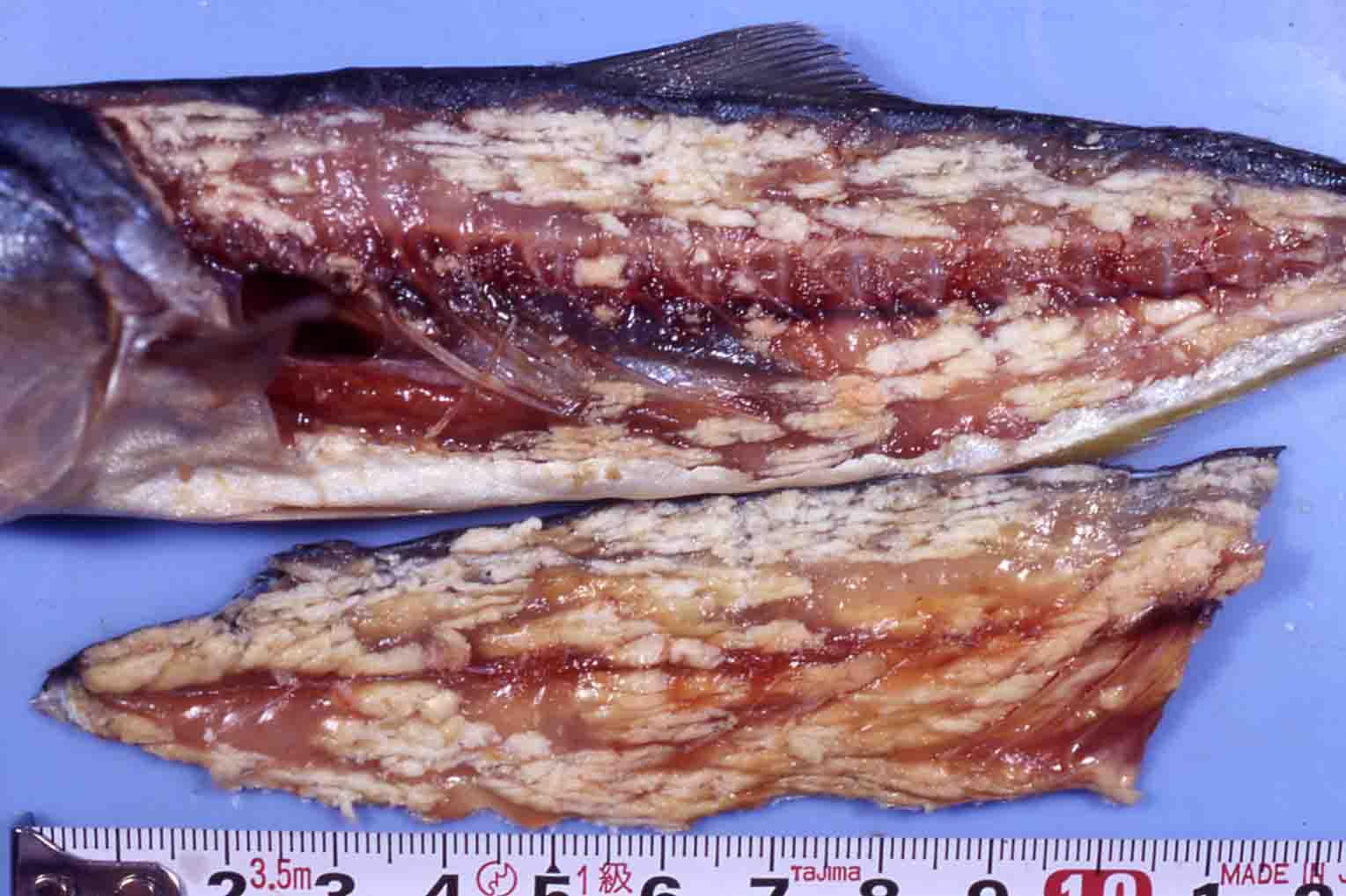
写真3.Microsporidium seriolaeの胞子